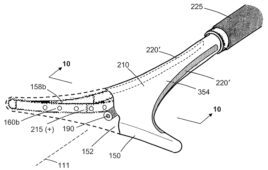
Symplicity Spyral肾去神经系统将能量传递给通往肾脏的神经,有助于调节血压。[图片由美敦力提供]
BTIG和Truist Securities的分析师表示,美敦力正在寻求FDA批准这项可能价值数十亿美元的业务,他们对商业化、报销和医生接受度有了新的疑问。
虽然Symplicity Spyral治疗降压药患者被证明是安全的,并显示出具有统计学意义和临床意义的办公室收缩压降低,但该治疗未能达到其主要疗效终点。
BTIG分析师Ryan Zimmerman和Sam Durno在给客户的一份报告中说:“令人惊讶的更新是,该试验在24小时动态收缩压(ABPM)方面没有显示出统计学意义,因为假对照组显示出血压意外下降,这主要是由于药物变化有利于降低血压。”“虽然这令人惊讶,但我们认为MDT解释了假对照组内的细微差别,这些结果并没有影响MDT围绕其RDN项目建立的丰富临床数据。尽管多项试验没有显示出统计学意义(HTN-3和ON MED),但我们认为RDN仍然被证明是安全有效的,并在数十亿美元的市场机会中作为药物管理的替代方案。”
相关:什么是肾去神经?美敦力冠脉和RDN总裁Jason Weidman解释道
Truist的分析师Richard Newitter、David Rescott、Samuel Brodovsky和Lin Zhang表示,“令人失望的”未达到终点对RDN来说并不是致命的打击,“但这可能意味着开发市场、获得报销和推动广泛的医生接受——当然前提是FDA批准。”
美敦力的Symplicity Spyral试验为何未能达到主要终点
美敦力向投资者提供了最新的RDN结果,并表示由于大流行和参与研究的患者的药物变化,Symplicity Spyral试验未能显著优于虚假对照组。
BTIG分析师说:“MDT将错过主要疗效终点归因于covid前和covid期间人群基线24小时ABPM模式的显著差异,以及由于不平衡的药物变化而导致扩展队列中血压的更大下降。”MDT强调,80%的扩展队列随访发生在COVID大流行期间。”
美敦力表示,扩大队列中的患者显著改变了药物摄入量,较高比例的假手术患者增加了药物摄入量,而较高比例的接受RDN治疗的患者减少了药物摄入量。
美敦力的Symplicity Spyral RDN治疗的商业化和报销
BTIG的分析师说,他们对美敦力解释为什么试验错过了主要终点感到满意,但他们仍然不清楚Symplicity Spyral的商业化和报销情况,假设FDA批准。
美敦力的高管列出了在美国报销的三种可能途径:
- 一个全国覆盖的决定
- 与七个医疗保险管理承包商(mac)合作
- 创新技术的报销由医疗保险和医疗补助服务中心(CMS)根据潜在的新兴技术过渡覆盖(TCET)计划.
BTIG分析师表示:“对于私人支付者来说,报销可能会在支付者的基础上建立,但我们认为,考虑到遗漏的统计终点,这将更具挑战性,可能需要上市后的数据。”
FDA的批准和RDN市场的下一步是什么?
美敦力表示,已将最新结果作为Symplicity Spyral上市前批准包的最终模块提交给FDA进行审查和批准。BTIG分析师表示,如有必要,该公司正准备将射频导管技术提交给FDA专家组,预计将在2023年的前三个月进行更新。
Truist的分析师表示,批准最早可能在2024年获得,但FDA专家组可能会将批准时间再推迟一年。
“除了我们在试验中证明的一致的绝对血压下降外,来自美敦力关键研究的长期数据——在今年的两份重要出版物中得到了强调《柳叶刀》-也证明了RDN的持久性和'永远在线'的效果,”美敦力高级副总裁兼冠状动脉和肾脏去神经总裁杰森·韦德曼在新闻发布会上说.“今天公布的ON MED结果是我们广泛的安全性和有效性证据概要的补充。有了这些结果,我们向FDA提交了PMA包,其中包括来自SPYRAL HTN临床项目的全部可用证据。我们很高兴有可能将这一重要的手术带给数百万需要的美国患者。”
美敦力的RDN市场机会有多大?
美敦力的领导人也表示有信心,1%的市场渗透率将带来10亿美元的商机。他们此前估计,到2026年,全球市场收入至少为5亿美元,到2030年为20 - 30亿美元,但在最新结果公布后,他们没有重申这些目标。
Truist的分析师表示:“由于缺乏统计意义,任何收入贡献的轨迹和最终规模都不确定。”
美敦力目前至少有四个RDN项目——Pulsar、G4、Helyx和GOAT——技术更新包括新的干预措施和能源。
两家公司都维持对美敦力股票的评级:BTIG为中性,Truist为持有。MDT股价今日下跌近5%,接近午盘时约为81.22美元。相比之下,MassDevice的Medtech100指数当天上涨了1%左右。