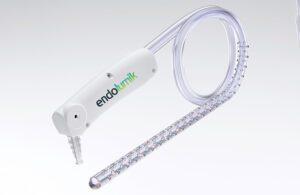
胃校准管在减肥过程中发射近红外光以增强能见度。
Endolumik的故事开始于几年前,当时FDA对内部外科订书机的风险发出了警告。
2019年,联邦机构警告医疗保健提供商,从2011年到2018年,它已经收到了超过4.1万份与外科订书机和内用订书钉有关的医疗设备报告。这些mdr记录了超过3.2万起故障,至少9000人重伤,366人死亡。
两年后,FDA提高了与订书机相关的风险级别,将设备从I类重新分类为II类,并对其进行上市前审查和特殊控制。
减肥外科医生诺娃·绍卡(Nova Szoka)已经在研究一种可以预防这些伤害的设备。她设想了一种照明胃校准管,可以用近红外光照射胃组织和脂肪。这种摄像头可见的荧光将使人们更容易看到病人体内的管子,降低了外科医生在减肥手术中穿孔或将管子固定在胃上的风险。
2020年,Szoka与马拉·麦克法登(Mara McFadden)共同创立了Endolumik,后者现任这家总部位于西弗吉尼亚州摩根敦的设备开发商的首席执行官。2022年,他们根据新的安全技术计划(STeP)向FDA提交了他们的设备今年获得了该机构的第一个STeP授权.
Szoka说:“安全永远是最重要的。医疗设计及外包.
FDA的STeP计划

Endolumik联合创始人Nova Szoka博士(左)和首席执行官Mara McFadden(图片由Endolumik提供)
STeP还加快了审查时间,但针对的是治疗或诊断不那么严重的疾病或状况的设备。FDA对这两个项目的目标是,比该机构单独的传统途径更快地为患者提供更安全、更好的设备。
FDA表示:“不符合突破性设备计划的医疗设备的进步,但在治疗和/或诊断不太严重的疾病或病症方面具有显著的安全优势,也可以为公众健康带来重要的好处。将于2021年推出STeP.“提高安全性的努力与提高整体临床效益直接相关,也可能帮助患者减少严重不良事件的发生。”
医疗设备开发人员可以通过Q-Submission申请加入自愿计划。然后,他们将与FDA合作,制定上市许可的最佳路径,无论是上市前批准、从头批准还是510(k)。
根据设备和放射健康中心的年度报告,FDA去年在30份申请中接受了14份STeP申请。
迈出一大步

使用近红外摄像机可以通过胃组织和脂肪看到Endolumik胃校准管。[图片由Endolumik提供]
麦克法登在一次采访中说:“我们发现他们在及时、互动的评估方面反应非常积极。”“有时候你会听到一些可怕的故事,即提交的内容会被搁置90天,然后你才会听到更多内容,但这并不是我们的经验。他们很快就回复了我们,我们有机会进行互动交流。”
麦克法登说,医疗设备开发商应该清楚地了解STeP的资格要求,并准备深入讨论他们的设备如何提高安全性。
她说:“证明自己更安全绝非小事。”“你必须至少展示四个不同因素中的一个。您可以减少已知不良事件的发生,减少已知故障模式的发生,减少已知用户危险或用户错误的发生,或者提高另一台设备的安全性。你真的必须做足功课,并准备好深入谈论你将如何对安全产生影响。”
麦克法登建议从监管顾问那里获得STeP请求和510(k)提交的帮助。Endolumik使用了由前FDA审查员Michael Nilo领导的Nilo医疗咨询集团。
“新型II类医疗设备的流程并不总是像510(k)计划看起来那么简单,”尼罗说。“FDA在为创新、更安全的设备设立项目方面做得很好,这可以帮助开发人员更好地接触到审查团队,并鼓励合作。我建议开发人员研究所有的程序并尝试一下。他们可以自由申请,最糟糕的结果是你被引荐给了你即将共事的审查团队。”
创造一个“金发女孩完美”平衡管
麦克法登说,Endolumik的合同制造商Virtec Medical是不可或缺的。设计该设备的最大挑战是平衡灵活性和刚性。
如果太硬,设备就不能安全地通过喉咙,可能会在食道或胃上穿孔。麦克法登说,如果太软,这个设备在到达胃之前就会“像意大利面一样弯曲”。
试错过程始于猪和尸体测试中的第一个3D打印原型。
麦克法登说:“在外径和电腔尺寸方面保持我们所需的功能尺寸的平衡,并获得正确的横截面以获得我们想要的机械性能——屈曲和扭结阻力之类的东西——从一开始就比我想象的要多迭代。”“这是我们最大的意想不到的挑战之一。”
该管由类似pvc的材料制成,其中一个管腔用于近红外led,另一个管腔用于吸力,以便外科医生根据需要清除胃液。为了确定合适的材料和尺寸,该团队不仅对现有的胃管进行了硬度计测试,还找到了“金发女孩完美”的平衡。
她说:“我们的工程团队真的分解了这种设备的不同特征:扭结压力、扣压、扭曲压力——基本上是量化所有这些东西,然后再输入。”
在最后的尸体实验室,团队邀请了一些外科住院医生来试一试。
“一旦我能够看到一些以前从未使用过设备的学员安全地介绍它,我就觉得我们已经准备好在临床试验中使用人类级别的设备了。”
Szoka说,到目前为止,Endolumik的临床试验已经治疗了22名患者,没有任何不良结果。
Endolumik的下一步是什么
Endolumik公司的荧光胃管是一种一次性设备。未来改进的一个目标是可持续性设计,包括提高可回收性。
虽然麦克法登拒绝透露该公司的其他可能性,但她提到了手术室中越来越多的近红外摄像机,这些摄像机可以让外科医生在未来使用Endolumik设备时更好地观察情况。
麦克法登说:“这确实促使我们开始长期而认真地思考,在微创手术的世界里,还有哪些地方会因为没有一个很好的工具视线而产生危险。”“我们在研发过程中肯定还有另一款令我们非常兴奋的产品,我们认为它可以解决解剖学上的一个同等甚至更大的痛点。”
“我们认为这是数字手术工具革命的开始,我们能够利用今天手术室里的工具,今天手术室里的塔,为外科医生提供先进的视觉效果,”她继续说。“随着更多的数字手术工具进入市场,我们很高兴能成为下一个行业的一员,看看下一代相机能做什么。”




告诉我们你的想法!
你一定是登录发表评论。