当涉及到软件作为一种医疗设备,监管环境非常复杂。
戴夫,票总理的研究

(图片来自Pixabay)
卫生服务提供者越来越部署SaMDs促进患者的疼痛治疗、心律失常管理、和血糖监测。一些应用程序需要每日使用的病人,有时一天多次,而剩余的符合良好的临床实践。潜在的优势包括减少办公室访问,增加了病人的频率指标,实时提醒如果阅读软件显示病人的风险。另一方面,SaMD的使用可能会导致较少的面对面接触病人,临床试验操作的潜在影响和长期护理。
在一个复杂的监管环境
SaMD相当复杂的监管环境,与多个通路影响最终的监管的决心和产品开发的影响。在分类SaMD复杂性反映了内在的挑战,作为调节这个新类需要一个基本的了解它是什么。国际医疗器械监管机构论坛(IMDRF)是一个全球性的工作小组由美国食品和药物管理局的代表,欧洲药品局和其他关键的监管机构。它将SaMD定义为“软件企业用于一个或多个医疗目的,执行这些目的不硬件医疗设备的一部分。“换句话说,软件组件必须通知或使医疗决定的结果,但不能主要驱动硬件设备。例如,通过定义,使用的医疗设备软件查看磁共振成像(MRI)扫描的图片在一个的电话将SaMD,但是软件使MRI机器运行测试不会有影响。
然而,假设一个设备检索信息,组织数据,并优化流程(请参见图1中的极左列)或使闭环干预没有临床中介(极右列)。在这种情况下,这不是SaMD,根据IMDRF。中间一个巨大的灰色地带,强调早期的重要性与监管机构达成共识的讨论最合适的类别为一个特定的设备。
图1所示。IMDRF分类模式的软件作为一个医疗设备(SaMD)
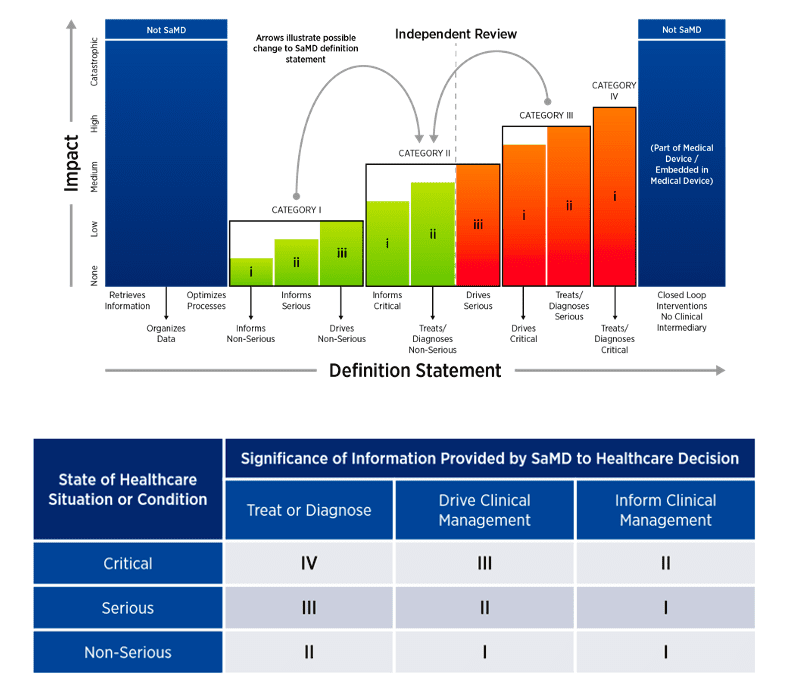
资料来源:美国食品和药物管理局。软件作为一种医疗设备(SAMD):临床评价指导。(图片由过犹不及
弥合差距在知识和法规
监管机构在不同地区有不同的见解的SaMD相关风险,并协调他们的规章制度创新的压力继续以惊人的速度增长。此外,SaMDs可以在线获得没有医疗监督,和病人可以使用它们在国外旅行时,规定可能会有所不同。这样的差距还有很多个人的解释与小于最优监管知识。引人注目的一个适当的平衡的挑战是鼓励创新,确保患者安全。
应对这一挑战,美国食品药品管理局已启动一个试点项目,数字医疗软件Precertification计划,提供更具流线型和基于软件的医疗设备的有效监管。另一个关键规定,IEC 82304 - 2016,描绘了软件产品一般健康安全要求。EMA同样调节软件驱动或影响设备的使用;如果软件是独立于任何其他设备,这是机密的。
抓住这个机会
在我们的估计,目前的监管环境为SaMD开发人员提供了一个难得的机会来塑造这些产品是如何管理的。使其极其重要的早期参与对话与监管机构,以确保清晰和协议设备分类。同样重要的是要遵循和有助于IMDRF决定,因为所有的主要监管机构认识到这个论坛。此外,在设计控制可以使灵活性监管区域和减少任何潜在的补救工作。最后,这些策略可以使全面了解适当的监管途径SaMD并有助于确保一个成功的市场。
戴夫是发展战略的副总裁在票总理的研究。
这篇文章的观点是作者的,不一定反映的MedicalDesignandOutsourcing.com或其雇员。




