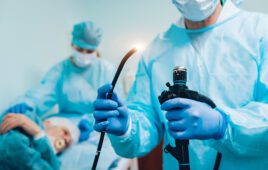
FDA希望一次性范围减少潜在致命的超级细菌感染。这是波士顿科技使它如何发生的。

提升模型D(图片由波士顿科学)
所以发生,波士顿科技公司已经致力于一个一次性的范围。
现在市场上,高举正在进医生的办公室,但它是一个复杂的旅程。
布莱恩·邓肯博士,波士顿科学的首席医疗官的内窥镜检查部门,最近告诉医疗设计与外包该公司克服了五个挑战使高举一个现实:
1。预测未来。
“整个动力开发这项技术的观察内镜社区的一些暴发感染的病人,”邓肯说。研究人员知道暴发来自耐药生物,但是他们没有数据来理解问题的严重性。“我们必须预测未来一点,因为数据是通过不同的途径,这是完全有可能的,它可能会说,这不是一个大问题。”
没有是这样的。结果是,FDA想远离完全可重复使用的范围。
2。设计要求
波士顿科学的设计过程是艰巨:基于150名医生的反馈,该公司设计了一个范围,经历了约9000次迭代。当完成时,处理器连接到相机盒包含2000个零件,和范围本身已经超过150人。花了六个生产设施和200建造设备的开发团队。
用最简单的术语来描述,邓肯所说:“我们需要这工作像一个最先进的可重用的范围,并将其转化为一次性设备。”
波士顿科学还必须解决错综复杂的设备如何导航在内镜逆行胰胆管造影(ERCP),要求过程,需要专门的范围有不同的特性。
“它看起来不只是前面,看起来,所以有不同的镜头角度。电梯机制,当我们把工具通过它,我们可以将这些工具更加精致时尚,”邓肯说。
邓肯说,还有另一个重要的考虑因素:“作为endoscopist如果它改变我的技术,我不会采取它。”
所以波士顿科学专家交谈,问:“这是正确的吗?是这样吗?我们必须使自己的模型,内镜逆行胰胆管造影,因为没有人有一个可以使用,”邓肯说。波士顿科学测试,然后在动物实验室,最终在人类以确保设备按预期执行。
3所示。成本
波士顿科学官员考虑所有相关的成本和可重用的范围,比如清洁,训练,和监控,搬到创建一个一次性设备和强有力的价值主张。
“如果成本类似于一个可重用的成本范围,这不会帮助你一定,因为我每天都不扔掉,范围,”邓肯说。加强命题,波士顿科技工作与CMS,门诊医生得到额外的报销手续。该公司在8月2日宣布,它也获得了额外的医疗保险住院治疗费用。
“你会得到使用范围。你会得到一个额外的支付,以抵消成本的范围。给我们,说明医疗保险已经做出了决定,“我们认为这是一个足够重要的问题,我们希望我们的患者管理这项技术,”邓肯说。
4所示。性能
简而言之,它必须工作,工作得很好。
“你必须使设备可以完成这项工作,不妥协的过程,给病人带来更多的问题。然后你必须让人们相信,它可以做这项工作,他们必须看到的价值,”邓肯说。
5。专业发展
波士顿科学很快发现它不需要训练人们在内镜逆行胰胆管造影;它需要得到卫生服务提供者理解感染问题。“很有可能,我可能会觉得我从未见过的患者感染污染范围,”邓肯说。
但他指出,感染后不要立即呈现,可能需要数周或数月出现在病人。感染甚至可能出现在一个没有直接连接到内镜逆行胰胆管造影。医疗社区需要更好地理解感染问题,过渡到新技术的需要
对于那些想要把一个设备变成一个一次性模型中,邓肯这个建议:“你必须让这些设计要求,你有做迭代与你工作的专家,这样你就不会浪费时间去错误的途径,不会让你你需要去的地方。
雷Marcano开始了他的职业生涯是一个长期的记者覆盖健康和医学。他是前总统的社会职业记者,两届普利策陪审员,富布赖特学者。