FDA今天发布了一份通知,称其正在评估新策略,以减轻与加热器-冷却器设备相关的感染。
FDA今天发布了一份通知,称其正在评估新策略,以减轻与加热器-冷却器设备相关的感染。
根据请注意在美国,政府正在与专业协会、公共卫生合作伙伴、加热器-冷却器制造商和专家合作,研究在医疗和外科手术过程中用于给病人加热或冷却的加热器-冷却器设备的相关问题。尽管回路中的流体不直接接触患者,但受污染的流体有可能进入设备的其他部分,或通过设备的排气口或其他未密封的开口通过空气传播细菌,到达环境和患者。
之前关于这些设备也出现过一些问题,包括LivaNova的3T加热器-冷却器设备.2016年,FDA警告病人和医生一种细菌感染的风险已关联设备。同年晚些时候,美国疾病控制与预防中心宣布警告有严重细菌感染的风险在开胸手术患者中使用3T加热器-冷却器。
LivaNova是美国制造和销售这些设备的三家公司之一,FDA的报告认为其清洁、消毒和雾化“足够”,而另外两家公司CardioQuip和Gentherm Medical的结果仍在等待。
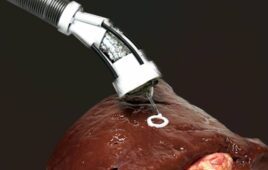
作为推动这一领域创新的一部分,FDA批准了光谱医疗”量子冷热器和兼容Qura量子PureFlow热交换器将于2022年5月上市。该设备不使用水,而是调节基于乙二醇的传热流体(HTF)的温度,然后该液体进入PureFlow热交换器以调节患者循环血液的温度,通过抑制细菌的生长来降低设备污染的风险,这已被确定为此类设备的问题根源。
FDA对该问题的分析已经确定,该问题的潜在根本原因包括非结核分枝杆菌(NTM)细菌通过空气通过雾化过程传播。另一个潜在原因是与该设备的排气风扇有关的层流中断(一种工程控制,旨在通过减少手术过程中的空气污染物来保护手术室环境)。
此外,由于大多数加热器-冷却器的设计是相似的,一些包含空气过滤器和水过滤器,而另一些没有。一些设备上的空气过滤器不足以捕获NTM细菌,而大多数设备上的风扇可能会促进雾化的NTM从设备内部进入手术室,并可能进入无菌手术区。
FDA表示:“根据该机构多年来审查再加工设备的经验,以及该机构和其他机构进行的研究,FDA确定了促进下一代可重复使用医疗设备创新的设计。”“这些设计特点有助于清洁和消毒,并减少污染和雾化的可能性。
“FDA将继续与制造商、医疗机构和公共卫生专家合作,评估加热-冷却器设备的新设计功能。”